• Các phản ứng có hại được báo cáo ở bệnh nhân viêm xương khớp và bệnh nhân viêm khớp dạng thấp với tỷ lệ mới mắc lớn hơn 0,01% và cao hơn so với tỷ lệ được báo cáo đối với giả dược trong 12 thử nghiệm lâm sàng có đối chứng với giả dược và/ hoặc thuốc có hoạt chất kéo dài đến 12 tuần với liều celecoxib hàng ngày từ 100 mg lên đến 800 mg. Trong các nghiên cứu bổ sung sử dụng chất so sánh NSAID không chọn lọc, khoảng 7.400 bệnh nhân viêm khớp đã được điều trị bằng celecoxib với liều hàng ngày lên đến 800 mg, trong đó có khoảng 2300 bệnh nhân được điều trị trong 1 năm hoặc lâu hơn. Các phản ứng bất lợi quan sát được với celecoxib trong các nghiên cứu bổ sung này phù hợp với các phản ứng đối với bệnh nhân viêm xương khớp và viêm khớp dạng thấp được liệt kê trong Bảng 1.
• Các phản ứng có hại được báo cáo với tỷ lệ xuất hiện cao hơn giả dược cho những đối tượng được điều trị bằng celecoxib 400 mg mỗi ngày trong các thử nghiệm phòng ngừa polyp dài hạn kéo dài đến 3 năm (thử nghiệm Phòng ngừa u tuyến bằng Celecoxib (APC) và Phòng ngừa Polyp dị dạng lẻ tẻ đại trực tràng (PreSAP); xem phần 5.1, An toàn tim mạch - các nghiên cứu dài hạn liên quan đến bệnh nhân có polyp tuyến rải rác).
• Các phản ứng có hại của thuốc từ giám sát sau lưu hành được báo cáo là tự phát trong một khoảng thời gian với ước tính có > 70 triệu bệnh nhân được điều trị bằng celecoxib (các liều lượng, thời gian và chỉ định khác nhau). Mặc dù đây được xác định là phản ứng từ các báo cáo hậu tiếp thị, dữ liệu thử nghiệm đã được tham khảo để ước tính tần suất. Tần suất dựa trên phân tích tổng hợp tích lũy với tổng hợp các thử nghiệm thể hiện mức độ tiếp xúc ở 38.102 bệnh nhân.
- xem Bảng 1.
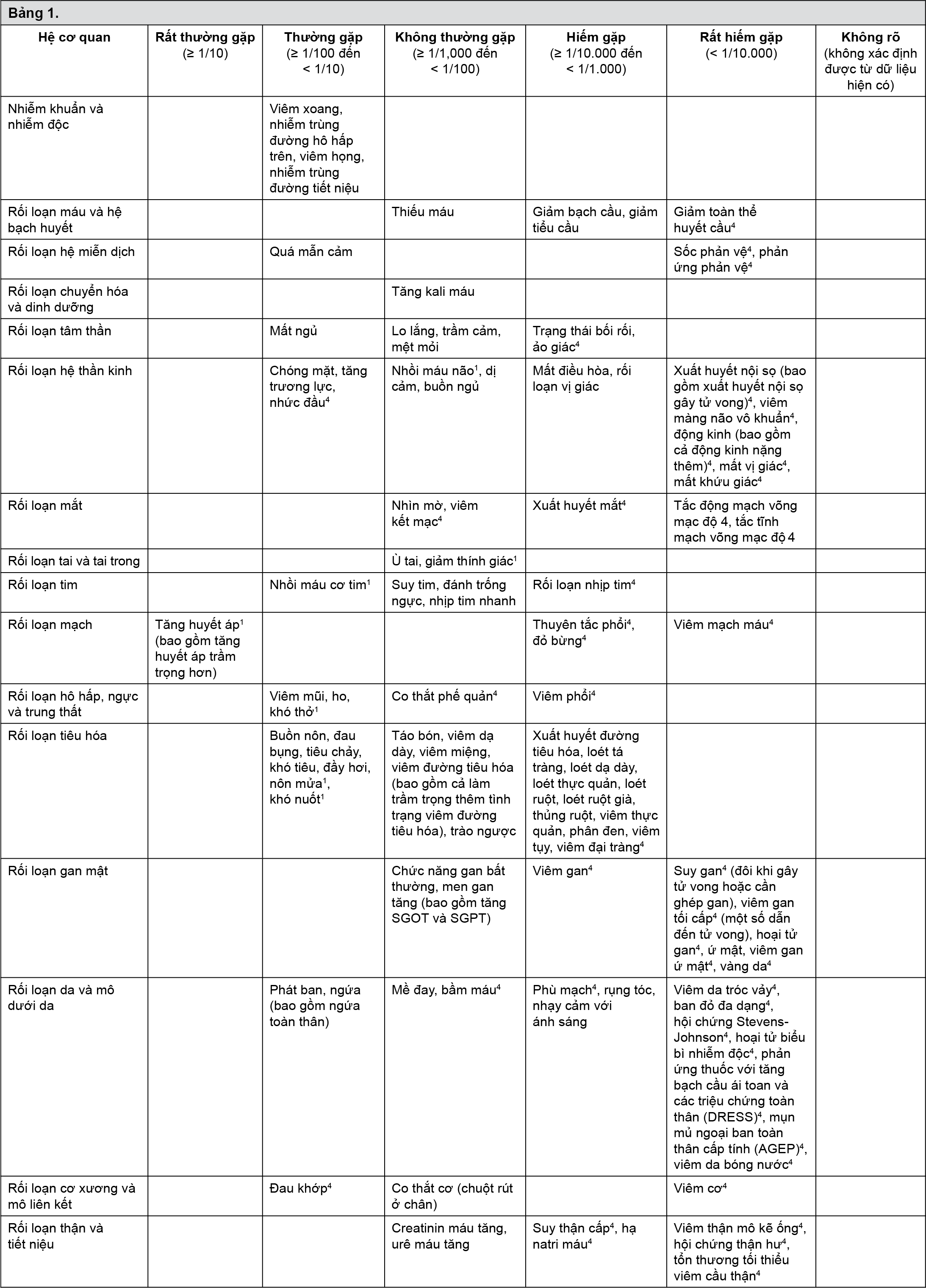
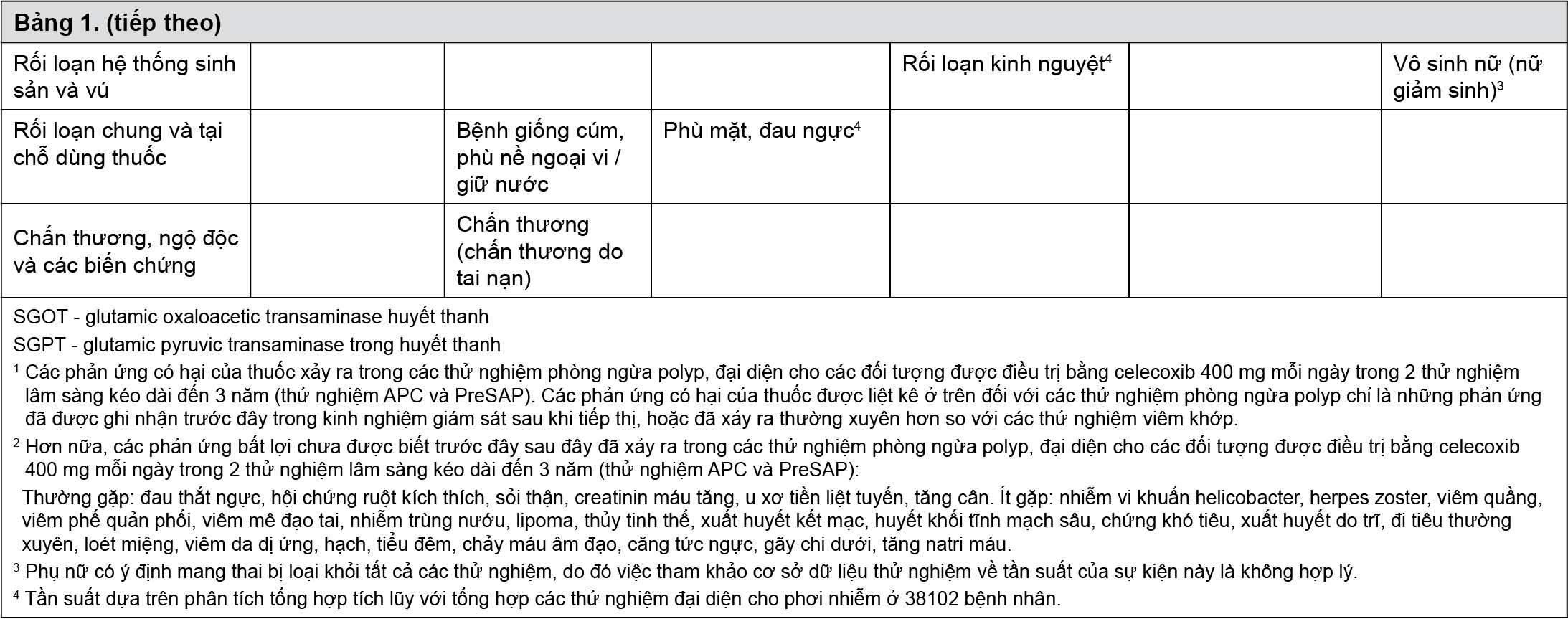
Trong dữ liệu cuối cùng (được công bố) từ các thử nghiệm APC và PreSAP ở những bệnh nhân được điều trị bằng celecoxib 400 mg mỗi ngày trong tối đa 3 năm (dữ liệu tổng hợp từ cả hai thử nghiệm; xem phần 5.1 để biết kết quả từ các thử nghiệm riêng lẻ), tỷ lệ vượt trội so với giả dược đối với nhồi máu cơ tim là 7,6 biến cố trên 1.000 bệnh nhân (không phổ biến) và không có tỷ lệ đột quỵ (không phân biệt loại) vượt quá so với giả dược.
View ADR Reporting Link





 Đăng xuất
Đăng xuất

